2021年7月23日, 国家药品监督管理局(NMPA)正式批准由上海济煜医药科技有限公司代理申报的磷酸索立德吉胶囊在国内上市。这是中国首个批准用于治疗局部晚期基底细胞癌(Basal Cell Carcinoma,BCC)的靶向药物,将为广大BCC患者和家庭提供全新的治疗选择。

“磷酸索立德吉胶囊”药品批准文号:国药准字HJ2021006
中文商品名:奥昔朵®/英文商品名:ODOMZO®
关于磷酸索立德吉胶囊
磷酸索立德吉胶囊(Sonidegib Phosphate Capsule)是一款口服Hedgehog(Hh)通路抑制剂,用于治疗不宜手术或放疗,以及手术或放疗后复发的局部晚期基底细胞癌(laBCC)成年患者。Hh信号通路作为一条经典的细胞信号通路,控制着胚胎发育及组织再生,其异常激活可能会诱发多种癌症。磷酸索立德吉可与Hh信号转导通路的跨膜蛋白Smoothened(SMO)结合,并对其产生抑制,从而发挥抗肿瘤作用。
Hedgehog通路[1]
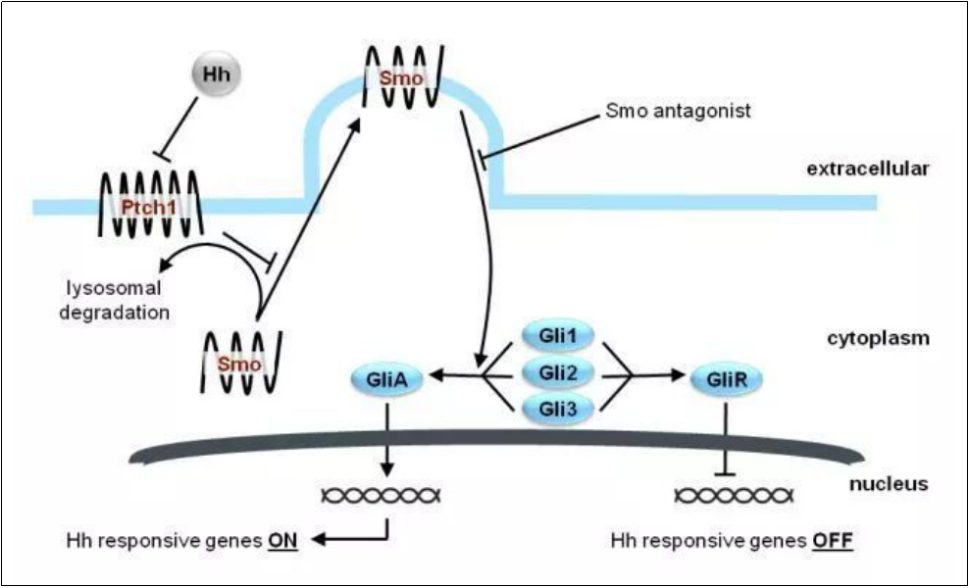
2015年7月24 日,磷酸索立德吉获得美国FDA加速批准上市 ,用于治疗手术或放疗后复发的laBCC,或不能手术或放疗的BCC患者;2015年8月14 日在欧盟获准上市。2016年12月太阳药业(SUN PHARMA)宣布以1.75亿美元从诺华(Novartis)获得该药全球权益。
2018年11月,国家药品监督管理局药品审评中心(CDE)将磷酸索立德吉纳入第一批临床急需境外新药名单。2020年1月,济民可信集团与太阳药业达成合作,获得磷酸索立德吉胶囊在大中华区(包括中国大陆、香港特别行政区、澳门特别行政区及台湾)的开发及商业化权益。2021年2月,上海济煜医药科技有限公司递交磷酸索立德吉的新药上市申请,3月初被CDE纳入优先审评,并在5个月内获得批准,实现了本品在国内快速获批上市。
关于BOLT研究
此次磷酸索立德吉国内获批,是基于一项名为BOLT(NCT01327053)的国际多中心、随机、双盲II期研究[2],该研究在230例局部晚期基底细胞癌(laBCC,n=194)或转移性基底细胞癌(mBCC,n=36)成人患者中开展,评估了磷酸索立德吉的有效性和安全性,研究对象来自12个国家的58个研究中心。患者按2:1比例随机接受口服磷酸索立德吉 800 mg或200 mg,每日1次。研究结果显示,第30个月时,随机接受每日200mg磷酸索立德吉治疗的laBCC患者客观缓解率(ORR)为56.1%,完全缓解率(CR)为21.2%,中位缓解持续时间为26.1个月,2年总体生存率(OS)为93.2%,且200mg的安全性要优于800mg。
关于基底细胞癌
基底细胞癌是最常见的皮肤肿瘤,约占非黑素瘤性皮肤肿瘤的80%,其中相当一部分患者(包括局限性的晚期BCC和转移性BCC)因长期缺乏临床治疗药物,面临高度毁容并可能危及生命。随着Hedgehog 通路在BCC 发生及发展中的机制得以揭示,新型药物Hedgehog通路抑制剂如磷酸索立德吉得到了充分的开发与应用,为BCC 的临床治疗带来了巨大的发展[3],为BCC患者带来了希望与福音!
关于上海济煜医药科技有限公司
上海济煜医药科技有限公司为济民可信集团全资子公司,负责该集团新药研发的规划与实施,遵循“以创新为引领、患者需求为导向”的理念,致力于成为具有全球影响力的药物研发中心,其研发管线涵盖生物大分子创新药、化学小分子创新药、新型中药、复杂仿制及高端制剂。
济民可信集团创建于1999年,总部位于中国南昌,产品管线覆盖肾病、肿瘤、心脑血管、呼吸抗感染、疼痛五大疾病领域,致力于为患者提供高质量的药品和创新医药解决方案。作为中国领先的大型现代制药集团之一,济民可信集团连续多年位列中国医药工业百强前十。
参考文献
[1] Medscape网站:https://www.medscape.org/viewarticle/750440
[2] Lear JT, et al. Long-term efficacy and safety of sonidegib in patients with locally advanced and metastatic basal cell carcinoma: 30-month analysis of the randomized phase 2 BOLT study. J Eur Acad Dermatol Venereol. 2018 Mar;32(3):372-381.
[3] 戴洁等.以Hedgehog信号通路为靶向治疗皮肤基底细胞癌的研究进展[J].临床皮肤科杂志,2020,49(12):762-764









